DE:
Dieser Earthcache wird euch zu einer kleinen, versteckten Tropfsteinhöhle in den Gärten von Malonas bringen.
Hier wird nur der Weg zur Tropfsteinhöhle beschrieben. Eine Rundtour steht im Rother oder Kosmos Wanderführer. Sowohl die beschriebene Tour mit Rückweg als auch die Rundtour sind ca. 4 km lang.
Bei Nässe sind die Felsen vor der Tropfsteinhöhle sehr rutschig. Dann sollte die Höhle nur von unten betrachtet werden. Die Aufgaben sind auch von dort zu lösen. Der Weg direkt vor den Eingang der Höhle sollte nur bei trocknen Felsen begangen werden. Den Zugang in die Höhle sollten nur Geübte wagen (dann ist es T 5).
Der Zugang zur Tropfsteinhöhle ist etwas versteckt und wird deshalb etwas genauer beschrieben:
An der Kapelle folgt man der Piste an der linken Mauer für ca. 20 min. Bei „(Nur für Wegfindung)1“ macht die Piste eine 180°-Kehre. Hier geht man den Pfad nach links Richtung Fluss. Am Fluss angekommen folgt man dem Bachlauf am Punkt „Weg zum Höhleneingang“ vorbei, bis es nicht mehr weiter geht. Von dort kann man rechts oben die Höhle schon sehen. Um zum Höhleneingang zu gelangen, geht man kurz zum Punkt „Weg zum Höhleneingang“ zurück und steigt kurz höhlenseitig den Hang aufwärts. Auf der Anhöhe umläuft man die Höhle, um oberhalb über einige Felsbrocken ins Bachbett abzusteigen und sich im Bachbett von oben der Höhle zu nähern.

Wie entstehen Tropfsteine und Tropfsteinhöhlen?
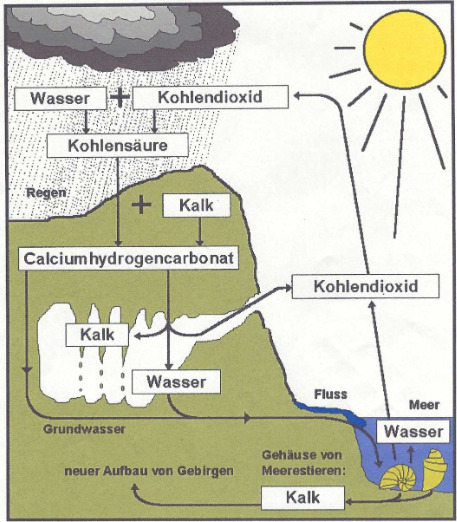
Die Salze der Kohlensäure, die Carbonate und Hydrogencarbonate, sind weit verbreitet. In Form von Kalk bilden sie ganze Gebirge (Alpen, Dolomiten, Schwäbische Alb) und Riffe. Sie sind auch für die Bildung von Tropfsteinen in Höhlen verantwortlich. Doch welche Reaktionen laufen hier genau ab?
Regenwasser nimmt etwas Kohlenstoffdioxid (CO2) entweder aus der Luft auf oder aus dem Boden auf (im Boden sind ca. 2 % CO2, in der Luft ca. 0,03 %). Dabei entsteht eine saure Lösung (Kohlensäure) - wie Mineralwasser, die in tiefe Risse und Spalten sickert und dort mit Kalkgestein reagiert und dieses auflöst, wobei das lösliche Salz Calciumhydrogencarbonat entsteht:
Kalk(gestein) + Wasser + Kohlenstoffdioxid –> Calciumhydrogencarbonat
CaCO3 + H2O + CO2 –> Ca(HCO3)2
Mit der Zeit werden die vorhandenen Risse und Spalten im Kalkgestein immer größer, bis sich schließlich Höhlen bilden.
Wenn nun versickertes Wasser mit dem gelösten Calciumhydrogencarbonat, umgangssprachlich nennen wir dieses auch “hartes Wasser”, von der Decke einer solchen Höhle tropft, entstehen langsam Tropfsteine – also neue Kalkablagerungen, weil das Calciumhydrogencarbonat wieder zerfällt:
Calciumhydrogencarbonat –> Kalk + Wasser + Kohlenstoffdioxid
Ca(HCO3)2 –> CaCO3 + H2O + CO2
Während der Tropfsteinbildung gasen also CO2 und Wasser aus – es ist keine Verdunstung, sondern eine echte chemische Reaktion – und der feste, kristalline Kalk (CaCO3) fällt wieder aus.
Von der Höhlendecke wächst ein Stalaktit, wenn nur sehr wenig Wasser tropft und der Tropfen ganz lange Zeit an der Höhlendecke hängen bleibt. Wenn viel “hartes Wasser” vorhanden ist und schwere Tropfen von der Höhlendecke herabfallen, entstehen am Höhlenboden stehende Stalagmiten. Beim Auftreffen des Tropfens am Höhlenboden entweicht dann ebenfalls aus dem harten Wasser Kohlenstoffdioxid und der weiße Kalk bleibt übrig. Somit bilden sich Jahr für Jahr hauchdünne Kalkschichten, die ein Kalendarium der Vergangenheit entstehen lassen. Dort wo Wasser sehr langsam und auch unregelmäßig an den Wänden und am Boden der Höhle entlangfließt, können sogenannte Flowstones entstehen. Auch bei deren Bildung gast aus dem Wasser Kohlenstoffdioxid aus und dünne flächige Kalkschichten lagern sich immer wieder auf der Oberfläche des Gesteins ab. Auch diese Schichten können im Laufe der Zeit eine beachtliche Dicke erreichen.
Wovon hängt es ab, ob Tropfsteine schnell oder langsam entstehen?
Manche Tropfsteine wachsen bis zu fünf Millimeter im Jahr, andere brauchen dafür 5000 Jahre. Hier sind einmal drei Faktoren, die die Wachstumsgeschwindigkeit eines Tropfsteins begünstigen:
-
viel CO2 im Boden ist gut: Je mehr CO2 sich im versickerten Wasser löst, desto saurer ist die entstehende Lösung und desto mehr Kalk löst sie wiederum auf. Das Wasser ist dann um so härter und hartes Wasser bildet dann gute Tropfsteine.
-
wenig CO2 in der Höhle ist gut: Je weniger CO2 in der Höhle ist, desto besser kann CO2 aus dem harten Wasser ausgasen. Das chemische Gleichgewicht erklärt das dann.
-
warme Höhlen sind gut: Je wärmer es in der Höhle ist, desto leichter gast das CO2 aus dem harten Wasser aus und der Kalk fällt aus. Chemikern wird das Prinzip von Le Chatelier hier bestimmt was sagen.
Warum sollte man keine Tropfsteine berühren?
An den Fingern ist Fett – Talg aus den Hautdrüsen. Am Tropfstein wird sich dieses Fett absetzen und daran wird das Wasser abperlen. An dieser Stelle wird sich dann kein weiterer Kalk mehr absetzen. Also: Finger weg!
Fragen:
1. Schätze die Breite und Höhe des Höhleneingangs ab.
2. Wie groß sind ungefähr die längsten Stalagtiten, die du erkennen kannst.
3. Nenne, welche Art von Tropfsteinen hier zahlenmäßig am häufigsten vorkommt und erkläre in eigenen Worten, warum das so ist.
4. Welche Tropfsteinformation überwiegt an den Wänden und auf dem Boden der Höhle? Welche Farbe hat diese?
5. Mache ein Foto mit dir oder einem persönlichen Gegenstand vor der Höhle. Alternativ reicht auch eine Skizze des Höhleneingangs.
Sende bitte alle Antworten an mein Profil. Sollte etwas nicht stimmen melde ich mich.
Ihr dürft sofort Loggen!
EN:
This Earthcache will take you to a small, hidden stalactite cave in the gardens of Malonas.
Only the path to the stalactite cave is described here. A round tour is in the Rother or Kosmos hiking guide. Both the tour described with the way back and the round tour are approx. 4 km long.
When wet, the rocks in front of the stalactite cave are very slippery. Then the cave should only be viewed from below. The tasks can also be solved from there. The path directly in front of the entrance to the cave should only be used when the rocks are dry. Only experienced people should venture into the cave (then it is T 5).
Access to the stalactite cave is somewhat hidden and is therefore described in more detail:
At the chapel, follow the piste along the left wall for about 20 minutes. At "(Only for pathfinding)1" the piste makes a 180° turn. Here you follow the path to the left towards the river. Arriving at the river, follow the course of the creek past the point "Path to the cave entrance" until you can go no further. From there you can already see the cave on the top right. To get to the cave entrance, go back to the point "Way to the cave entrance" and climb up the slope on the cave side. On the hill you walk around the cave in order to descend over some boulders into the creek bed and approach the cave from above in the creek bed.

How are stalactites and stalactite caves formed?
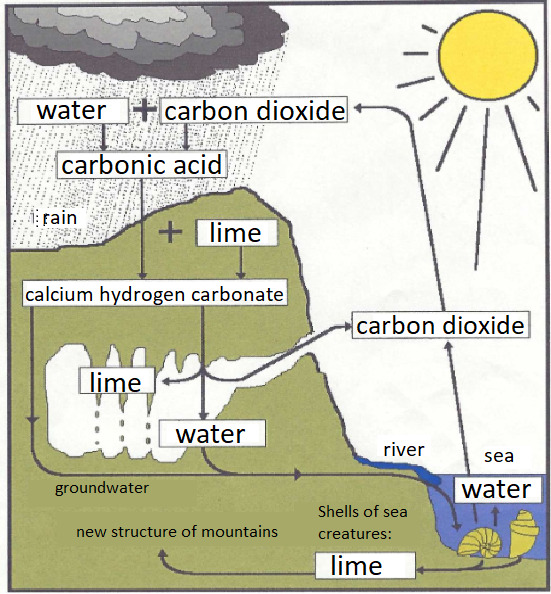
The salts of carbonic acid, the carbonates and hydrogen carbonates, are widespread. In the form of limestone, they form entire mountain ranges (Alps, Dolomites, Swabian Alb) and reefs. They are also responsible for the formation of stalactites in caves. But what exactly are the reactions here?
Rainwater absorbs some carbon dioxide (CO2) either from the air or from the soil (there is about 2% CO2 in the soil, about 0.03% in the air). This produces an acidic solution (carbonic acid) - like mineral water, which seeps into deep cracks and crevices, where it reacts with limestone and dissolves it, forming the soluble salt calcium hydrogen carbonate:
Lime (rock) + water + carbon dioxide –> calcium bicarbonate
CaCO3 + H2O + CO2 –> Ca(HCO3)2
Over time, the existing cracks and crevices in the limestone become larger and larger until caves eventually form.
When seeped water drips from the ceiling of such a cave with the dissolved calcium bicarbonate, colloquially we also call it "hard water", stalactites slowly form - i.e., new lime deposits, because the calcium bicarbonate decomposes again:
Calcium bicarbonate –> lime + water + carbon dioxide
Ca(HCO3)2 –> CaCO3 + H2O + CO2
During stalactite formation, CO2 and water outgas – it is not evaporation, but a real chemical reaction – and the solid, crystalline lime (CaCO3) precipitates again.
A stalactite grows from the cave ceiling if very little water drips and the drop sticks to the cave ceiling for a very long time. When there is a lot of "hard water" and heavy drops fall from the cave ceiling, stalagmites standing at the bottom of the cave are formed. When the drop hits the cave floor, carbon dioxide also escapes from the hard water and the white lime remains. Thus, year after year, wafer-thin layers of limestone are formed, creating a calendar of the past. So-called flowstones can form where water flows very slowly and irregularly along the walls and floor of the cave. When they are formed, carbon dioxide is released from the water and thin, flat layers of lime are repeatedly deposited on the surface of the rock. These layers can also reach a considerable thickness over time.
What determines whether stalactites are formed quickly or slowly?
Some stalactites grow up to five millimeters a year, others need 5000 years to do so. Here are three factors that favor the growth rate of a stalactite:
-
a lot of CO2 in the soil is good: the more CO2 dissolves in the seeped water, the more acidic the resulting solution is and the more lime it dissolves. The water is then all the harder and hard water then forms good stalactites.
-
little CO2 in the cave is good: The less CO2 there is in the cave, the better CO2 can outgas from the hard water. The chemical equilibrium then explains this.
-
warm caves are good: the warmer it is in the cave, the easier it is to outgas the CO2 from the hard water and the lime precipitates. Chemists will certainly find the principle of Le Chatelier to say something here.
Why shouldn't you touch stalactites?
On the fingers is fat – sebum from the skin glands. This fat will settle on the stalactite and the water will roll off it. No further lime will settle at this point. So: hands off!
Questions:
1. Estimate the width and height of the cave entrance.
2. Approximately how big are the longest stalactites you can see.
3. Name which type of stalactite is the most common here and explain in your own words why that is.
4. Which stalactite formation predominates on the walls and floor of the cave? What color is this?
5. Take a picture with you or a personal item in front of the cave. Alternatively, a sketch of the cave entrance is sufficient.
Please send all answers to my profile. If something is wrong, I'll let you know.
You can log immediately!